中国科学院微生物研究所,中国微生物学会,中国菌物学会
文章信息
- 周萍萍, 王涛, 孙元, 仇华吉. 2021
- Pingping Zhou, Tao Wang, Yuan Sun, Hua-Ji Qiu. 2021
- cGAS-STING信号通路:免疫监视的重要机制
- cGAS-STING signaling pathway: important mechanisms of immune surveillance
- 微生物学报, 61(7): 1882-1895
- Acta Microbiologica Sinica, 61(7): 1882-1895
-
文章历史
- 收稿日期:2020-08-13
- 修回日期:2020-11-10
- 网络出版日期:2021-02-03
先天免疫系统作为第一道防线,利用模式识别受体(pattern recognition receptors,PRRs)识别细胞外或细胞内病原微生物相关分子模式(pathogenassociated molecular patterns,PAMPs)。对于细胞外病原微生物,包括Toll样受体(Toll-like receptors,TLRs)和C型凝集素受体(C-type lectin receptors,CLRs)在内的跨膜受体是主要的感受器[1],这些受体的信号域位于细胞质,与配体结合后启动信号级联反应,产生一系列与免疫和炎症反应有关的基因产物。当病原微生物进入细胞并在细胞内复制时,激活不同信号通路的细胞质感受器。例如,核苷酸结合寡聚域(NOD)样受体(nucleotidebinding oligomerization domain (NOD)-like receptors,NLRs)的感受器可以激活炎性小体,通过识别各种微生物分子、毒素和损伤的细胞触发下游信号通路,诱导炎症反应以及白细胞介素1β (IL-1β)和白细胞介素18 (IL-18)的分泌[2];胞质RIG-I样受体(RIG-I-like receptors,RLRs)通过识别细胞质中的病毒双链RNA (double-stranded RNA,dsRNA)触发信号级联,导致I型干扰素和炎症细胞因子的产生[3]。环磷酸鸟苷-腺苷酸合成酶(cyclic guanosine monophosphate-adenosine monophosphate synthase,cGAS)是一种细胞DNA感受器,主要识别双链DNA (double-stranded DNA,dsDNA)激活先天性免疫应答,包括诱导干扰素的表达等[4]。
众所周知,DNA携带从病毒到人类等生物体的遗传信息。在证实DNA承载遗传信息以前,人们发现它可以刺激免疫应答,例如吞噬细胞的招募[5]。免疫系统对微生物DNA的识别为检测各种各样的病原微生物提供了一个通用的机制,因为除了RNA病毒外,所有的微生物在其生命周期中都包含并需要DNA。在真核细胞中,DNA存在于细胞核和线粒体中,细胞质中基本不存在自体DNA。微生物感染细胞后将DNA运输到细胞质,进而激活先天免疫系统,在一定的病理条件下,自体DNA在细胞质中积累,导致自身组织的自身免疫性攻击。一般来说,免疫系统不能识别自体DNA,但吞噬细胞吞噬死的肿瘤细胞后可以检测到肿瘤源DNA,这为肿瘤的先天免疫和抗肿瘤免疫的激活提供了一种机制。本文将讨论cGAS-STING通路在免疫防御含DNA病原微生物中的调控作用与功能,在自身免疫性疾病中的应答转归以及病原微生物逃逸cGAS-STING信号通路的策略。
1 cGAS-STING信号通路cGAS包含一个核苷酸转移酶结构域和两个主要的DNA结合结构域[6],在无DNA的情况下,cGAS处于自抑制状态[7–11],当cGAS与DNA结合时,cGAS与DNA结合形成一个2:2的二聚体[7–8],诱导活性位点的改变,并催化三磷酸腺苷(adenosine triphosphate,ATP)和三磷酸鸟苷(guanosine triphosphate,GTP)合成环鸟苷酸腺苷酸(cyclic guanosine monophosphate adenosine monophosphate,cGAMP)。cGAMP功能是作为第二信使结合内质网(endoplasmic reticulum,ER)膜蛋白干扰素刺激因子(stimulator of interferon genes,STING),并诱导构象改变激活STING[12–13]。然后,活化的STING从ER到高尔基体中间室和高尔基体间进行转运[14–15],在此过程中,STING的羧基末端招募并激活TANK结合激酶1 (TANK-binding kinase 1,TBK1),使干扰素调节因子3 (interferon regulatory factor 3,IRF3)磷酸化,磷酸化的IRF3二聚化并进入细胞核[16–18]。STING也激活激酶Iκκ,使核因子κB (nuclear factor-kappa B,NF-κB)的抑制剂IκB家族磷酸化,磷酸化的IκB蛋白通过泛素-蛋白酶体途径被降解[19],此时NF-κB进入细胞核,与IRF3等干扰素调节因子共同作用(图 1),诱导干扰素和炎性细胞因子如TNF、IL-1β和IL-6的表达。
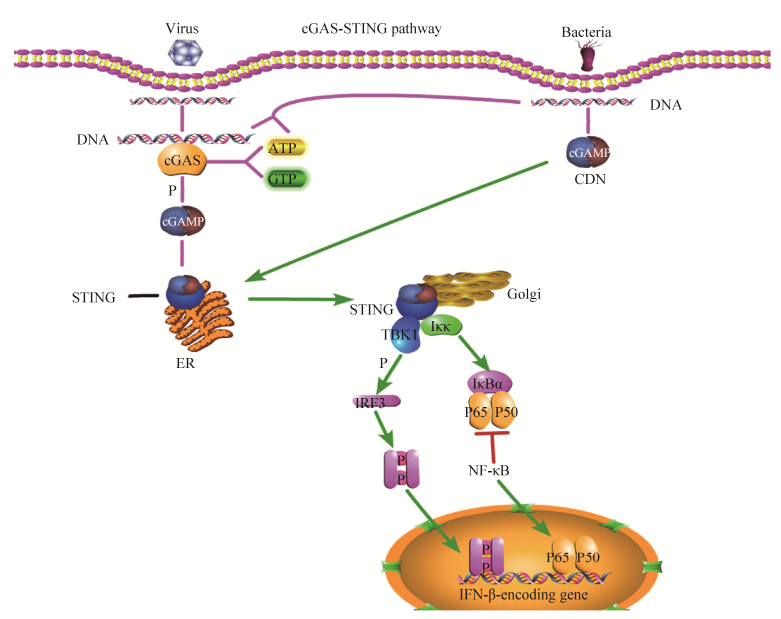
|
| 图 1 cGAS-STING信号通路示意图 Figure 1 Schematic diagram of cGAS-STING signal pathway. Viruses and bacteria are dangerous pattern of molecules. Cytoplasmic DNA binds and activates cGAS to catalyze ATP and GTP synthetic 2', 3'-cGAMP, which combines with the ligand STING of ER, transports to the Golgi apparatus, then IKK and TBK1 are activated. TBK1 is phosphorylated by activation of STING, and IRF3 is then phosphorylated by TBK1. Phosphorylated IRF3 forms a dimer and enters the nucleus, which along with NF-κB activates the expression of type I interferon and other immune regulatory molecules. |
1.1 cGAS的活化
cGAS被dsDNA激活不依赖于DNA序列[6]。cGAS-dsDNA复合物的晶体结构表明,cGAS与dsDNA的糖-磷酸骨架结合而不与任何碱基结合,说明cGAS的激活与DNA序列无关[7–8, 10–11]。DNA碱基的损伤,如紫外线照射引起的氧化,并不损害或增强DNA激活cGAS的能力,但氧化后的DNA对细胞核酸酶的抗性更强,从而诱导更强的干扰素表达。dsRNA可以与cGAS结合,但不能激活cGAS[20]。建模研究表明,B型dsDNA与cGAS的活化环结合并调控活化环,导致活化位点的重新排列,相比之下,A型dsRNA无法调控cGAS的活化环,这可能是RNA无法活化cGAS的原因[7]。短的dsDNA (长度约为15 bp)足以在体外结合并激活cGAS,但较长的DNA需要激活细胞内的cGAS通路,可能是因为细胞内存在核酸酶和其他调节因子。
1.2 翻译后修饰对cGAS活化的调节虽然cGAS活化的主要机制是通过其与dsDNA的结合,但还存在其他机制来调节cGAS通路。为了调节对外来物的强烈而敏感的应答并确保有机体对自身DNA无应答,cGAS通过翻译后修饰对其酶活性进行调控。小鼠cGAS被Akt激酶磷酸化后抑制了cGAS的活性,表明cGAS通路和其他调控Akt的通路之间可能存在相互作用[21]。微管蛋白聚谷酶TTLL4和TTLL6使cGAS发生谷氨酰胺化抑制cGAS的活性,羧基肽酶CCP5和CCP6逆转这种修饰后激活cGAS活性[22]。在这两种情况下,只有部分cGAS蛋白被磷酸化或谷氨酰胺化修饰所抑制,在此提出这样一个问题:这种修饰是如何影响未被修饰的cGAS活性的?目前相关研究不清楚,有待进一步挖掘。
1.3 cGAS的转录和表观遗传调控编码cGAS的基因是由干扰素诱导的,这为cGAS通路的激活放大提供了一种正反馈机制[23–24]。许多肿瘤细胞系已经失去了cGAS的表达,因此在DNA刺激或DNA病毒感染时产生干扰素和细胞因子方面存在缺陷。在这些细胞中,cGAS表达的抑制可以通过DNA甲基化抑制剂逆转,这表明,编码cGAS的基因表达是通过表观遗传机制沉默的[25]。
1.4 STING的活化STING在氨基末端有4个跨膜结构域,将蛋白锚定在ER膜上,大的羧基结构域位于细胞质中。无论是否存在配体,STING都会在ER膜上形成二聚体,一个cGAMP分子通过疏水作用和氢键作用与一个STING二聚体的中心缝隙结合,导致STING构象发生变化[13, 26],释放一个羧基末端尾部(carboxyl-terminal tail,CTT),招募和激活TBK1,但在STING晶体结构中看不到STING的CTT。通过分子建模和功能分析,有人提出,cGAMP结合STING形成的盖子结构提供了一个与STING羧基末端结合的锚定位点,这导致CTT形成类似于TBK1底物的结构,从而使TBK1磷酸化STING的CTT,而这对IRF3的激活非常重要[27]。
cGAMP结合STING后不久,STING激活Iκκ和TBK1,继而分别激活NF-κB和IRF3。TBK1通过丝氨酸和苏氨酸残基磷酸化STING,包括第366位的丝氨酸。这种STING的磷酸化对随后TBK1磷酸化IRF3至关重要[28]。磷酸化的STING结合到IRF3的一个带正电的区域,通过TBK1招募IRF3进行磷酸化。一旦IRF3被磷酸化,它会形成一个同型二聚体进入细胞核,诱导干扰素的表达。值得注意的是,包括MAVS、TRIF和STING在内的几个先天免疫的接头分子都具有一个高度保守的基序(℗p-Leu-X-Ile-Ser,其中℗-表示磷酸基团,X表示任何氨基酸),且在受到同源配体的刺激时发生磷酸化。这些接头分子的磷酸化为TBK1磷酸化IRF3提供了一种许可机制,这一机制确保了在所有能够激活TBK1的因子中,只有少数,如病毒感染会导致IRF3的激活和干扰素的表达,这也是防止产生过量的干扰素、避免自身免疫性疾病的一个重要机制。也有人提出STING的第366位丝氨酸磷酸化会导致STING的降解和cGAS-STING信号通路的失活[29]。然而,将STING的第366位丝氨酸突变为丙氨酸后,在DNA或cGAMP的刺激下仍然会发生降解,说明第366位丝氨酸并非关键位点。多项研究表明,STING也受泛素化调控,至少有3种不同的已证实E3泛素连接酶对STING的活化起正调控作用,E3泛素连接酶TRIM32和TRIM56可以促进STING的第63位赖氨酸(K63)发生多聚泛素化,从而增强其下游通路的激活[30–31],定位在ER由AMFR-GP78和INSIG1组成的E3泛素连接酶复合物促进STING的K27多聚泛素化、TBK1的募集和干扰素的诱导[32]。相比之下,E3泛素连接酶RNF5和TRIM30a促进了STING的K48多聚泛素化,使其被蛋白酶体降解,最终导致DNA信号级联反应的抑制[33]。总之,泛素化在STING活化或失活中的作用较为复杂,需要进一步研究不同类型泛素化和E3泛素连接酶在体内对STING通路的作用。
1.5 STING转运和降解的调节STING与cGAMP结合后迅速从ER转运至核周区,形成大的点状结构[18]。ARF GTPase抑制剂布雷菲德菌素A抑制STING的转运进而阻断下游通路的激活[29],说明STING的转运对信号通路激活起重要作用。志贺氏菌的效应蛋白IpaJ使GTPase的ARF家族失活,从而阻止STING从ER-高尔基体中间区到高尔基体的转运,因此抑制STING诱导的干扰素产生。STING的第88和91位半胱氨酸在高尔基体被棕榈酰化,通过使用化学抑制剂或突变两个半胱氨酸残基来抑制STING的棕榈酰化,从而阻止了STING的活化[34]。STING完成其信号功能后,可能通过自噬作用迅速降解[25],据报道,自噬激酶ULK1-ATG1可能参与了STING的降解,但STING靶向自噬途径的机制尚不清楚。
1.6 其他调节因子在发现cGAS作为激活干扰素通路的胞质DNA感受器之前,一些其他的蛋白质被提出作为DNA感受器,包括DNA结合蛋白(DNA-dependent activator of IRFs,DAI)、DDX41 (DEAD-box helicase 41)、干扰素诱导蛋白16 (IFN-γ-inducible protein 16,IFI16/P204)等[35]。然而,这些蛋白在感知胞质DNA通路中的作用是有争议的,部分原因是没有一个基因被研究证实与此有关。DAI缺陷的小鼠可以对DNA刺激或DNA病毒感染产生正常的干扰素应答[36]。同样,通过CRISPR/Cas9技术缺失IFI16的人细胞对胞质DNA刺激会诱导正常的干扰素[37]。与这些假定的DNA感受器结果相反,cGAS的遗传缺失对转染DNA或感染含有DNA的病原微生物(包括DNA病毒、逆转录病毒和细菌),完全抑制了干扰素的产生。因此,cGAS在感知胞质DNA通路中诱导干扰素的产生具有非冗余的作用。
cGAS还可以与自噬调节因子beclin-1结合,这种相互作用通过与STING非依赖型的机制诱导自噬[38],cGAS与beclin-1的结合使beclin-1复合物释放自噬的负调节因子RUBICON,从而诱导自噬促进胞质中DNA的清除。
2 cGAS-STING信号通路的功能通过cGAS缺陷小鼠的遗传学方法表明cGAS是一种可以检测包含DNA的大量病原微生物的感受器,几乎能识别所有dsDNA并产生免疫应答。cGAS-STING信号通路在病毒、细菌、逆转录病毒感染中以及自身免疫性和炎性疾病中均发挥重要功能。
2.1 cGAS-STING信号通路在DNA病毒感染中的作用DNA病毒入侵机体后,dsDNA能够诱导机体产生免疫应答,诱导干扰素和其他炎症因子等的产生。cGAS识别入侵的病毒DNA,通过STING-TBK1信号通路启动针对多数DNA病毒(如单纯疱疹病毒(herpes simplex virus 1,HSV-1)、牛痘病毒(vaccinia virus,VACV)、腺病毒(adenovirus,Ad)、巨细胞病毒(cytomegalovirus,CMV)和卡波西肉瘤相关疱疹病毒(Kaposi’s sarcoma-associated herpesvirus,KSHV) 等的免疫应答反应,且依赖cGAS和STING诱导干扰素的产生[39–45]。机体感染HCMV后,激活间质细胞的cGAS-STING信号通路进而诱导产生I型干扰素,从而发挥抗病毒作用[39]。KSHV感染能够激活cGAS-STING信号通路,敲除cGAS和STING后抑制了KSHV感染的内皮细胞中IFN-β的活化,IRF3和TBK1的磷酸化水平也降低,使得从潜伏期激活的病毒数量增多。Cavlar等发现,敲除STING的细胞降低了IFN-β的产生;缺乏cGAS或STING的小鼠在受到HSV-1、小鼠γ疱疹病毒68或VACV感染时不产生IFN-β,且体内病毒滴度升高。cGAS和STING缺陷型小鼠对RNA病毒感染也更敏感[46],尽管缺少cGAS或STING的细胞在感染RNA病毒时会分泌正常的干扰素,可能是由于cGAS通路在稳态下产生少量干扰素,而这些干扰素对于抵抗DNA或RNA病毒的体内感染很重要。另外,体内感染RNA病毒可能导致细胞损伤和细胞死亡,导致细胞DNA暴露于细胞质中,从而激活cGAS通路,有助于防御RNA病毒感染。病毒粒子的膜融合也被认为可以激活cGAS通路,也有助于对RNA病毒的免疫防御[47]。Anghelina等发现,在cGAS和STING基因缺失的小鼠中,TBK1、IRF3的磷酸化水平显著降低,进而诱导的IFN-β、促炎症细胞因子减少,肝组织中抗病毒转录水平同样下降。这些研究表明,病毒感染后cGAS-STING通路作为主要的病毒DNA感受通路,诱导干扰素表达,引起细胞的免疫应答,发挥抗病毒作用,表明cGAS-STING信号通路在抗DNA病毒反应中至关重要。
2.2 cGAS-STING信号通路在RNA病毒感染中的作用cGAS是逆转录病毒(包括HIV-1和HIV-2)的关键感受器[48–50]。HIV的病毒衣壳进入巨噬细胞和树突状细胞(dendritic cells,DCs)后,病毒衣壳内的逆转录酶将病毒RNA转化为cDNA,cDNA被直接转移至细胞核并整合到宿主基因组中,因此,逆转录病毒通常不会引起强烈的先天性免疫反应。然而,如果病毒衣壳的完整性受到损害或如果阻止细胞质DNA积累的一些宿主因素(如SAMHD1、TREX1和CPSF6)失去功能,即cGAS可以识别细胞质中短的碱基配对DNA片段发挥免疫调节,从而触发干扰素和其他细胞因子的诱导表达[42]。除此之外,HIV病毒DNA也能被细胞多聚谷氨酰胺结合蛋白(polyglutamine-binding protein 1,PGBP1)识别。PGBP1的羧基端结构域与HIV病毒DNA结合,其氨基端WW结构域与cGAS相互作用,激活cGAS-STING信号通路。敲除PGBP1可大大降低HIV诱导DCs的免疫反应,同样,PGBP1突变的DCs对HIV的免疫应答能力降低。cGAS在检测逆转录cDNA中的作用已经扩展到内源性逆转录病毒和逆转录元件,缺乏cGAS或STING的小鼠不能对多价抗原(如细菌荚膜多糖)产生T细胞非依赖型的B细胞应答,这种抗原的免疫导致内源性逆转录病毒RNA在抗原特异性B细胞中上调[51]。RNA通过RNA解旋酶RIG-I和MAVS的途径被检测到,也被逆转录成cDNA,然后通过cGAS-STING途径被检测到,与单独敲除MAVS和cGAS相比,敲除MAVS和cGAS会导致B细胞反应中更严重的缺陷。因此,MAVS和cGAS对内源性逆转录病毒的检测具有重要意义,可促进B细胞产生抗体。综上表明,cGAS在逆转录病毒感染中发挥重要作用。
2.3 cGAS-STING信号通路在细菌感染中的作用细菌含有丰富的DNA,许多细菌可以侵入哺乳动物细胞,并在宿主细胞内复制[46]。细菌利用它们的分泌装置将效应分子传递到细胞质中,虽然尚不清楚细菌DNA是如何进入细胞质的,但许多细胞内的细菌通过cGAS-STING途径诱导干扰素产生。机体被细菌感染后,细胞内cGAS表达水平上调,识别并结合进入胞质的dsDNA,激活STING,引起下游细胞因子的产生,同时,cGAS还与胞质的其他DNA感受器发挥协同作用,共同调节干扰素和细胞因子的产生。在细菌(如结核分枝杆菌、单核李斯特氏菌、沙门氏菌等)感染cGAS或STING缺陷的小鼠骨髓源巨噬细胞中,IFN-β和细胞因子的产生急剧下降[52–54]。另外,有些细菌可以产生STING激动剂如环状二核苷酸(cyclic dinucleotides,CDNs),直接激活STING并诱导产生下游细胞因子。目前,经鉴定的可激活cGAS通路的细菌不断增加,包括分枝杆菌、李斯特氏菌、志贺氏菌、弗朗西斯氏菌、沙门氏菌、生脓链球菌、嗜肺军团菌、衣原体、奈瑟氏菌和B组链球菌[52–58],除了单核增生李斯特菌以一种依赖STING而不是cGAS的方式诱导小鼠巨噬细胞中干扰素产生外,在没有cGAS的情况下,大多数细菌对干扰素的诱导作用基本消失。虽然I型干扰素在病毒感染过程中能发挥稳定的病毒清除作用,但其在细菌感染过程中发挥的作用机制尚不明确,在某些情况下,甚至表现出对机体有害的一面,所以cGAS信号通路在细菌感染及清除过程中的作用有待进一步研究。
2.4 cGAS-STING通路在自身免疫性和炎性疾病中的作用虽然cGAS-STING信号通路已经演变为检测微生物感染的主要防御机制,但cGAS也同样受到自身激活的DNA触发自身免疫的威胁。任何从细胞核和线粒体释放或泄漏到细胞质的DNA都可能触发cGAS通路,cGAS通路与自身免疫性疾病之间的联系已经在Aicardi-Goutières综合征(Aicardi-Goutières syndrome,AGS)中得到证实。AGS是一组单基因自身免疫性疾病,主要特征是诱导I型干扰素的基因表达升高[59],通过对该综合征患者的遗传研究表明,其原因是几个关键基因的突变,包括TREX1、RNase H2、SAMHD1、腺苷脱氨酶ADAR1和细胞受体MDA5,这些疾病由于在缺乏TREX1或RNaseH2功能的小鼠中cGAS-STING通路被激活而导致[60–64]。TREX1是一种可降解有裂痕的dsDNA和单链DNA的外切酶[65],TREX1缺陷的小鼠,在出生后几个月内死于多器官炎症,尤其是心肌炎;而在缺乏TREX1的小鼠中,仅敲除编码cGAS或STING的基因的一个等位基因,在很大程度上使它们免于致命的自身免疫表型[60–62]。RNase H2能降解RNA-DNA杂交中的RNA,并去除在DNA复制过程中错误整合到dsDNA中的核糖。一个表达催化不活跃的RNase H2A突变体的敲除小鼠株,在围产期死亡,来自这些小鼠胚胎的原代细胞表现出干扰素刺激基因的表达升高,但这种表达通过cGAS或STING的缺失而被消除[63],删除STING可降低这些小鼠的围产期致死率。DNase II是在溶酶体中消化DNA的主要酶,它的缺失会导致小鼠胚胎死亡,因为胚胎中过多的I型干扰素会杀死红细胞,干扰素受体(interferonreceptor,IFNAR)的缺失降低了小鼠胚胎的致死率,但删除了TLR9或配体MyD88却不能。有趣的是,缺乏DNase II和IFNAR的小鼠会继发关节炎,这可能是由于持续产生炎性细胞因子所导致,在DNase-II缺陷小鼠中,cGAS或STING的缺失可以完全拯救它们从胚胎致死率、自身免疫和炎症中的表型[59]。总之,这些遗传学研究为cGAS通路的激活引起人自身免疫与炎症疾病提供了证据,为靶向cGAS-STING途径治疗某些人类自身免疫性和炎症性疾病提供了参考。
3 病原微生物逃逸cGAS-STING信号通路的策略 3.1 DNA病毒逃逸cGAS-STING信号通路的策略DNA杂合体和DNA病毒在介导宿主先天性免疫反应中发挥重要作用[61]。cGAS识别并结合病毒或异常定位的DNA后,催化产生的第二信使2’, 3’-cGAMP与STING结合,活化的STING二聚体从ER转移至高尔基体,随后招募TBK1和IRF3,促进IRF3的激活和同源二聚体形成,然后活化的IRF3易位到细胞核中并诱导I型IFN的表达。在转移到高尔基体之前,活化的STING激活NF-κB,诱导促炎性细胞因子的表达。在病原微生物和宿主之间持续的博弈斗争中,大多数微生物已经进化出成功躲避其易感宿主免疫系统攻击的方法,多种病毒进化出多种机制逃逸cGAS-STING信号通路介导的先天免疫,表 1归纳总结了不同DNA病毒蛋白针对cGAS-STING信号通路中以cGAS、STING为靶蛋白,发挥免疫逃逸作用的机制。
| DNA virus | Protein | Evasion of mechanism | Reference |
| KSHV | LANA | Interacting with cGAS to inhibit cGAS activity | [41] |
| ORF52 | Blocking the binding of DNA to cGAS directly to inhibit cGAS activity | [42] | |
| vIRF1 | Binding to STING to prevent its binding to TBK1 | [43] | |
| HSV-1 | VP22 | Interacting with cGAS to inhibit cGAS activity | [51] |
| UL37 | Making cGAS of human and mouse deamidation | [52] | |
| UL41 | Reducing the protein level of cGAS by degrading the mRNA level of cGAS | [53] | |
| VP11/12 | Interacting with cGAS to promote the degradation of STING | [54] | |
| VP1-2 | After deleting VP1-2 to induce STING signaling pathway | [55] | |
| ICP27 | Interacting with STING and TBK1 to inhibit IRF3 phosphorylated TBK1 | [66] | |
| HCMV | IE2 | Promoting degradation of STING by the proteasome pathway | [47] |
| UL82 | Blocking the translocation of STING complex to inhibit the downstream pathway of STING | [48] | |
| UL48 | Inhibiting ubiquitination of STING, and then completely blocking its activation | [49] | |
| M48 | Interacting with STING to prevent its interaction with TBK1 | [50] | |
| UL31 | Dissociating DNA from cGAS to inhibit the activation of cGAS | [56] | |
| UL83 | Inhibiting the activation of cGAS | [57] | |
| US9 | Interacting with STING to inhibit its dimerization and activation | [58] | |
| MHV68 | ORF64 | Inhibiting the activation of STING | [50] |
| MCMV | m152 | Delaying translocation of STING to inhibit the activation of antiviral signaling pathway | [50] |
| M48 | Interacting with STING to prevent its interaction with TBK1 | [59] | |
| HBV | Pol | Binding to STING and reducing the activity and function of its K63 polyubiquitin ligase | [60] |
| Adenovirus | E1A | Binding to STING by the LXCXE motif to inhibit its signal pathway | [67] |
| HPV | E7 | Binding STING by the LXCXE motif to inhibit its signal pathway | [67] |
3.2 RNA病毒逃逸cGAS-STING信号通路的策略
尽管cGAS-STING通路在识别DNA病毒中的作用比RNA病毒阐述得更清晰,但很多研究也证实,RNA病毒的复制与cGAS或者STING介导的抗病毒天然免疫反应具有密切的联系。RNA病毒编码的蛋白也能阻断cGAS-STING通路的激活。表 2归纳总结了不同RNA病毒蛋白针对cGAS-STING信号通路中以cGAS、STING为靶蛋白,发挥免疫逃逸作用的机制。主要包括黄病毒(yellow fever virus,YFV)、丙型肝炎病毒(hepatitis C virus,HCV)、登革热病毒(Dengue fever virus,DENV)、人冠状病毒(human coronavirus,HCoV)、猪流行性腹泻病毒(porcine epidemic diarrhea virus,PEDV)、非典型肺炎冠状病毒(severe acute respiratory syndrome coronavirus,SARS-CoV)。
| RNA virus | Protein | Evasion of mechanism | Reference |
| YFV | NS4B | Interacting with STING to inhibit the activation of STING-mediated signaling pathway | [61] |
| HCV | NS4B | Interacting with STING to destroy the formation of STING complex | [62] |
| DENV | NS2B/3 | Binding and cracking of STING | [63] |
| HCoV-NL63 | PLP2-TM | Interacting with STING to inhibit the formation of STING dimer and block the interaction of STING and TBK1 | [64] |
| PEDV | PLP | Binding STING to inhibit its ubiquitination | [65] |
| SARS-CoV | PLP | Inhibiting STING activity and negatively regulating its dimerization and ubiquitination | [68] |
3.3 其他病原微生物逃逸cGAS-STING信号通路的策略
对于病原微生物,避免触发cGAS途径的最常见和最有效的方法是将它们的DNA从细胞质中隐藏起来。对于HIV-1,细胞质中的病毒衣壳进一步招募宿主因子CPSF6和环亲蛋白。这些宿主因子有助于协调逆转录、衣壳脱衣和病毒整合前复合物进入细胞核,这样病毒DNA就不会暴露在细胞质中。CPSF6的缺失导致感染野生型HIV-1的巨噬细胞产生干扰素,同样,DNase Trex1的缺失导致HIV-1 DNA在细胞质中积累,从而通过cGAS诱导干扰素的产生[47]。细胞因子SAMHD1通过负调控干扰素表达,以限制DCs和巨噬细胞中HIV-1的感染[44–45]。然而,HIV-2编码Vpx通过CRL4-DCAF1复合物介导SAMHD1降解,导致DCs和巨噬细胞中HIV-2的复制[44–45]。HIV-1编码的衣壳保护其病毒cDNA免受DCs中cGAS的识别。这些结果表明,HIV-1与HIV-2协同选择宿主蛋白或编码逃逸蛋白以减少病毒DNA在细胞质中的暴露和积累,从而拮抗cGAS-STING通路的触发。
Andrade等研究发现,一些GBS菌株能够合成一种环二核苷酸磷酸二酯酶(cyclic dinucleotide phosphodiesterase,CdnP),从而抑制细菌感染后STING及下游通路的激活[52]。而志贺氏菌利用效应物IpaJ抑制ARF GTP酶活性,从而阻止STING的转运和激活[55]。
综上所述,病原微生物编码的蛋白可以靶向cGAS-STING通路中的不同因子,从而阻断信号的传递以及IFN的产生,最终逃脱宿主的抗病毒作用。
4 cGAS-STING信号通路研究的方向由于现阶段对天然免疫系统的认识有限,cGAS-STING通路是至今发现的为数不多的几条能够完整描绘诱导产生I型IFN过程的通路,其中仍有很多细节有待深入探索,在微生物感染和自身免疫性疾病的背景下,直接激活细胞质中cGAS的DNA的性质仍在很大程度上未知,控制cGAS活性、cGAMP稳定性以及STING的转运和降解的其他调控因子仍有待发现。还需要进一步的工作来了解STING是如何激活下游激酶和转录因子的,以及STING蛋白二聚的具体机制,激活STING蛋白的关键位点和机制等等。另一个有趣的研究领域是探索cGAS-STING通路与其他先天免疫系统通路之间的潜在相互调控作用。最后,关于IFI16和DDX41等其他DNA感受器在cGAS-cGAMP信号通路中的作用也是急需解决的问题。目前还不清楚cGAS是否在不同的细胞类型中起作用,或者这些不同的感受器是否在不同的细胞类型或组织环境中起作用。此外,IFI16或DDX41等感受器是否在cGAS-cGAMP系统发挥协同作用或直接参与诱导干扰素,仍有待进一步研究。虽然cGAS-STING通路的激活是复杂的,也没有得到很好的研究,但是在cGAS-STING通路激活的过程中,针对不同的接头分子或者配体可以开发调节剂,包括配体结合、移位和棕榈酰化等等,这些均为cGAS-STING信号通路的研究提供了借鉴与参考。
5 总结和展望遗传学和微生物学研究已经证实cGAS- STING通路在免疫防御多种DNA病毒、逆转录病毒和细菌方面的重要作用。本文主要介绍了cGAS-STING信号通路,及其在抗病毒天然免疫中主要的调控作用与功能,并对病原微生物逃逸此通路的策略进行了分析,将为相关研究与抗病毒药物的研发提供新的思路。
cGAS-STING通路在抗病原微生物感染中发挥重要作用,由于研究的不断探索与发现,推测cGAS感知的病原微生物范围会继续扩大,有可能涉及到真菌和寄生虫,因为它们也含有丰富的DNA。由于所有的细胞和组织中都含有DNA,这些DNA有可能成为引发炎症的潜在分子,所以cGAS通路的激活可能与许多重要器官的炎症性疾病有关。因此,cGAS通路可能在许多涉及炎症的常见疾病中发挥作用,所以开发针对cGAS-STING通路的有效且特异的抑制剂,这不仅是一种非常有用的研究工具,也是一种潜在的治疗手段。
cGAS-STING信号转导包含细胞内和细胞外的生物学过程,且具有异质性,影响cGAS-STING信号通路活化因素众多。例如,激活感受器的性质、强度和持续时间均可能影响着免疫应答。尽管这些过程复杂,但cGAS-STING信号通路的分子机制及其调节因子仍然是开发针对多种疾病的具有希望的靶点。
病毒在与宿主的“军备竞赛”中进化出多种策略,拮抗宿主的天然免疫反应,以利于自身的感染和复制。解析病毒免疫逃逸蛋白拮抗免疫反应的机制对于开发有效和持久的疫苗和抗病毒药物等领域至关重要;同时,挖掘病毒及其免疫逃避蛋白相互作用的宿主细胞,有希望开发基于细胞的药物靶点。虽然关于受感染细胞内cGAS和STING的功能仍有许多未被研究的地方,但RNA和DNA病毒使用许多不同的免疫逃避策略都表明了这一途径对于检测病毒病原微生物非常重要。一些RNA和DNA病毒采用相似的机制来抑制STING的功能,包括STING的降解。但病毒也存在免疫调节的功能,且病毒难以控制,所以我们对病毒感染和宿主先天性免疫反应之间的联系了解得越多,就越有可能开发出成功且有效的治疗方法。总之,更好地了解病毒与人类宿主之间的“战斗”将有利于病毒性疾病的预防和治疗。
| [1] | Pandey S, Kawai T, Akira S. Microbial sensing by Toll-like receptors and intracellular nucleic acid sensors. Cold Spring Harbor Perspectives in Biology, 2014, 7(1): a016246. |
| [2] | Broz P, Dixit VM. Inflammasomes: mechanism of assembly, regulation and signalling. Nature Reviews Immunology, 2016, 16(7): 407-420. DOI:10.1038/nri.2016.58 |
| [3] | Yoneyama M, Onomoto K, Jogi M, Akaboshi T, Fujita T. Viral RNA detection by RIG-I-like receptors. Current Opinion in Immunology, 2015(32): 48-53. |
| [4] | Cai X, Chiu YH, Chen ZJ. The cGAS-cGAMP-STING pathway of cytosolic DNA sensing and signaling. Molecular Cell, 2014, 54(2): 289-296. DOI:10.1016/j.molcel.2014.03.040 |
| [5] | Knight M, Braverman J, Asfaha K, Gronert K, Stanley S. Lipid droplet formation in Mycobacterium tuberculosis infected macrophages requires IFN-γ/HIF-1α signaling and supports host defense. PLoS Pathogens, 2018, 14(1): e1006874. DOI:10.1371/journal.ppat.1006874 |
| [6] | Sun LJ, Wu JX, Du FH, Chen X, Chen ZJ. Cyclic GMP-AMP synthase is a cytosolic DNA sensor that activates the type I interferon pathway. Science, 2013, 339(6121): 786-791. DOI:10.1126/science.1232458 |
| [7] | Zhang X, Wu JX, Du FH, Xu H, Sun LJ, Chen Z, Brautigam CA, Zhang XW, Chen ZJ. The cytosolic DNA sensor cGAS forms an oligomeric complex with DNA and undergoes switch-like conformational changes in the activation loop. Cell Reports, 2014, 6(3): 421-430. DOI:10.1016/j.celrep.2014.01.003 |
| [8] | Li X, Shu C, Yi GH, Chaton CT, Shelton CL, Diao JS, Zuo XB, Kao CC, Herr AB, Li PW. Cyclic GMP-AMP synthase is activated by double-stranded DNA-induced oligomerization. Immunity, 2013, 39(6): 1019-1031. DOI:10.1016/j.immuni.2013.10.019 |
| [9] | Kranzusch PJ, Lee ASY, Berger JM, Doudna JA. Structure of human cGAS reveals a conserved family of second-messenger enzymes in innate immunity. Cell Reports, 2013, 3(5): 1362-1368. DOI:10.1016/j.celrep.2013.05.008 |
| [10] | Motwani M, Pesiridis S, Fitzgerald KA. DNA sensing by the cGAS-STING pathway in health and disease. Nature Reviews Genetics, 2019, 20(11): 657-674. |
| [11] | Civril F, Deimling T, de Oliveira Mann CC, Ablasser A, Moldt M, Witte G, Hornung V, Hopfner KP. Structural mechanism of cytosolic DNA sensing by cGAS. Nature, 2013, 498(7454): 332-337. DOI:10.1038/nature12305 |
| [12] | Wu JX, Sun LJ, Chen X, Du FH, Shi HP, Chen C, Chen ZJ. Cyclic GMP-AMP is an endogenous second messenger in innate immune signaling by cytosolic DNA. Science, 2013, 339(6121): 826-830. DOI:10.1126/science.1229963 |
| [13] | Motwani M, Pesiridis S, Fitzgerald KA. DNA sensing by the cGAS-STING pathway in health and disease. Nature Reviews Genetics, 2019, 20(11): 657-674. |
| [14] | Ishikawa H, Ma Z, Barber GN. STING regulates intracellular DNA-mediated, type I interferon-dependent innate immunity. Nature, 2009, 461(7265): 788-792. DOI:10.1038/nature08476 |
| [15] | Dobbs N, Burnaevskiy N, Chen DD, Gonugunta VK, Alto NM, Yan N. STING activation by translocation from the ER is associated with infection and autoinflammatory disease. Cell Host & Microbe, 2015, 18(2): 157-168. |
| [16] | Tanaka Y, Chen ZJ. STING specifies IRF3 phosphorylation by TBK1 in the cytosolic DNA signaling pathway. Science Signaling, 2012, 5(214): ra20. |
| [17] | Fitzgerald KA, McWhirter SM, Faia KL, Rowe DC, Latz E, Golenbock DT, Coyle AJ, Liao SM, Maniatis T. IKK ε and TBK1 are essential components of the IRF3 signaling pathway. Nature Immunology, 2003, 4(5): 491-496. DOI:10.1038/ni921 |
| [18] | Sharma S, tenOever BR, Grandvaux N, Zhou GP, Lin RT, Hiscott J. Triggering the interferon antiviral response through an IKK-related pathway. Science, 2003, 300(5622): 1148-1151. DOI:10.1126/science.1081315 |
| [19] | Ishikawa H, Barber GN. STING is an endoplasmic reticulum adaptor that facilitates innate immune signalling. Nature, 2008, 455(7213): 674-678. DOI:10.1038/nature07317 |
| [20] | Gehrke N, Mertens C, Zillinger T, Wenzel J, Bald T, Zahn S, Tüting T, Hartmann G, Barchet W. Oxidative damage of DNA confers resistance to cytosolic nuclease TREX1 degradation and potentiates STING-dependent immune sensing. Immunity, 2013, 39(3): 482-495. DOI:10.1016/j.immuni.2013.08.004 |
| [21] | Seo GJ, Yang A, Tan B, Kim S, Liang QM, Choi Y, Yuan WM, Feng PH, Park HS, Jung JU. Akt kinase-mediated checkpoint of cGAS DNA sensing pathway. Cell Reports, 2015, 13(2): 440-449. DOI:10.1016/j.celrep.2015.09.007 |
| [22] | Xia PY, Ye BQ, Wang S, Zhu XX, Du Y, Xiong Z, Tian Y, Fan ZS. Glutamylation of the DNA sensor cGAS regulates its binding and synthase activity in antiviral immunity. Nature Immunology, 2016, 17(4): 369-378. DOI:10.1038/ni.3356 |
| [23] | Schoggins JW, Wilson SJ, Panis M, Murphy MY, Jones CT, Bieniasz P, Rice CM. A diverse range of gene products are effectors of the type I interferon antiviral response. Nature, 2011, 472(7344): 481-485. DOI:10.1038/nature09907 |
| [24] | Ma F, Li B, Liu SY, Iyer SS, Yu YX, Wu AP, Cheng GH. Positive feedback regulation of type I IFN production by the IFN-inducible DNA sensor cGAS. The Journal of Immunology, 2015, 194(4): 1545-1554. DOI:10.4049/jimmunol.1402066 |
| [25] | Xia TL, Konno H, Ahn J, Barber GN. Deregulation of STING signaling in colorectal carcinoma constrains DNA damage responses and correlates with tumorigenesis. Cell Reports, 2016, 14(2): 282-297. DOI:10.1016/j.celrep.2015.12.029 |
| [26] | Feng X, Liu DY, Li ZY, Bian JL. Bioactive modulators targeting STING adaptor in cGAS-STING pathway. Drug Discovery Today, 2020, 25(1): 230-237. DOI:10.1016/j.drudis.2019.11.007 |
| [27] | Tsuchiya Y, Jounai N, Takeshita F, Ishii KJ, Mizuguchi K. Ligand-induced ordering of the C-terminal tail primes STING for phosphorylation by TBK1. EBioMedicine, 2016(9): 87-96. |
| [28] | Liu SQ, Cai X, Wu JX, Cong Q, Chen X, Li T, Du FH, Ren JY, Wu YT, Grishin NV, Chen ZJ. Phosphorylation of innate immune adaptor proteins MAVS, STING, and TRIF induces IRF3 activation. Science, 2015, 347(6227): aaa2630. DOI:10.1126/science.aaa2630 |
| [29] | Konno H, Konno K, Barber GN. Cyclic dinucleotides trigger ULK1(ATG1) phosphorylation of STING to prevent sustained innate immune signaling. Cell, 2013, 155(3): 688-698. |
| [30] | Zhang J, Hu MM, Wang YY, Shu HB. TRIM32 protein modulates type I interferon induction and cellular antiviral response by targeting MITA/STING protein for K63-linked ubiquitination. Journal of Biological Chemistry, 2012, 287(34): 28646-28655. |
| [31] | Tsuchida T, Zou J, Saitoh T, Kumar H, Abe T, Matsuura Y, Kawai T, Akira S. The ubiquitin ligase TRIM56 regulates innate immune responses to intracellular double-stranded DNA. Immunity, 2010, 33(5): 765-776. DOI:10.1016/j.immuni.2010.10.013 |
| [32] | Zhong B, Zhang L, Lei CQ, Li Y, Mao AP, Yang Y, Wang YY, Zhang XL, Shu HB. The ubiquitin ligase RNF5 regulates antiviral responses by mediating degradation of the adaptor protein MITA. Immunity, 2009, 30(3): 397-407. DOI:10.1016/j.immuni.2009.01.008 |
| [33] | Wang YM, Lian QS, Yang B, Yan SS, Zhou HY, He L, Lin GM, Lian ZX, Jiang ZF, Sun B. TRIM30α is a negative-feedback regulator of the intracellular DNA and DNA virus-triggered response by targeting STING. PLoS Pathogens, 2015, 11(6): e1005012. |
| [34] | Mukai K, Konno H, Akiba T, Uemura T, Waguri S, Kobayashi T, Barber GN, Arai H, Taguchi T. Activation of STING requires palmitoylation at the Golgi. Nature Communications, 2016(7): 11932. |
| [35] | Paludan SR, Bowie AG. Immune sensing of DNA. Immunity, 2013, 38(5): 870-880. |
| [36] | Ishii KJ, Kawagoe T, Koyama S, Matsui K, Kumar H, Kawai T, Uematsu S, Takeuchi O, Takeshita F, Coban C, Akira S. TANK-binding kinase-1 delineates innate and adaptive immune responses to DNA vaccines. Nature, 2008, 451(7179): 725-729. |
| [37] | Gray EE, Winship D, Snyder JM, Child SJ, Geballe AP, Stetson DB. The AIM2-like receptors are dispensable for the interferon response to intracellular DNA. Immunity, 2016, 45(2): 255-266. |
| [38] | Liang QM, Seo GJ, Choi YJ, Kwak MJ, Ge JN, Rodgers MA, Shi MD, Leslie BJ, Hopfner KP, Ha T, Oh BH, Jung JU. Crosstalk between the cGAS DNA sensor and Beclin-1 autophagy protein shapes innate antimicrobial immune responses. Cell Host & Microbe, 2014, 15(2): 228-238. |
| [39] | Paijo J, Döring M, Spanier J, Grabski E, Nooruzzaman M, Schmidt T, Witte G, Messerle M, Hornung V, Kaever V, Kalinke U. cGAS senses human cytomegalovirus and induces type I interferon responses in human monocyte-derived cells. PLoS Pathogens, 2016, 12(4): e1005546. |
| [40] | Lio CWJ, McDonald B, Takahashi M, Dhanwani R, Sharma N, Huang J, Pham E, Benedict CA, Sharma S. cGAS-STING signaling regulates initial innate control of cytomegalovirus infection. Journal of Virology, 2016, 90(17): 7789-7797. |
| [41] | Zhang GG, Chan BC, Samarina N, Abere B, Weidner-Glunde M, Buch A, Pich A, Brinkmann MM, Schulz TF. Cytoplasmic isoforms of Kaposi sarcoma herpesvirus LANA recruit and antagonize the innate immune DNA sensor cGAS. Proceedings of the National Academy of Sciences of the United States of America, 2016, 113(8): E1034-E1043. |
| [42] | Wu JJ, Li WW, Shao YM, Avey D, Fu BS, Gillen J, Hand T, Ma SM, Liu X, Miley W, Konrad A, Neipel F, Stürzl M, Whitby D, Li H, Zhu FX. Inhibition of cGAS DNA sensing by a herpesvirus virion protein. Cell Host & Microbe, 2015, 18(3): 333-344. |
| [43] | Ma Z, Jacobs SR, West JA, Stopford C, Zhang ZG, Davis Z, Barber GN, Glaunsinger BA, Dittmer DP, Damania B. Modulation of the cGAS-STING DNA sensing pathway by γ-herpesviruses. Proceedings of the National Academy of Sciences of the United States of America, 2015, 112(31): E4306-E4315. |
| [44] | Li XD, Wu JX, Gao DX, Wang H, Sun LJ, Chen ZJ. Pivotal roles of cGAS-cGAMP signaling in antiviral defense and immune adjuvant effects. Science, 2013, 341(6152): 1390-1394. |
| [45] | Schoggins JW, MacDuff DA, Imanaka N, Gainey MD, Shrestha B, Eitson JL, Mar KB, Richardson RB, Ratushny AV, Litvak V, Dabelic R, Manicassamy B, Aitchison JD, Aderem A, Elliott RM, García-Sastre A, Racaniello V, Snijder EJ, Yokoyama WM, Diamond MS, Virgin HW, Rice CM. Pan-viral specificity of IFN-induced genes reveals new roles for cGAS in innate immunity. Nature, 2014, 505(7485): 691-695. |
| [46] | Portnoy DA, Auerbuch V, Glomski IJ. The cell biology of Listeria monocytogenes infection: the intersection of bacterial pathogenesis and cell-mediated immunity. Journal of Cell Biology, 2002, 158(3): 409-414. |
| [47] | Holm CK, Jensen SB, Jakobsen MR, Cheshenko N, Horan KA, Moeller HB, Gonzalez-Dosal R, Rasmussen SB, Christensen MH, Yarovinsky TO, Rixon FJ, Herold BC, Fitzgerald KA, Paludan SR. Virus-cell fusion as a trigger of innate immunity dependent on the adaptor STING. Nature Immunology, 2012, 13(8): 737-743. |
| [48] | Rasaiyaah J, Tan CP, Fletcher AJ, Price AJ, Blondeau C, Hilditch L, Jacques DA, Selwood DL, James LC, Noursadeghi M, Towers GJ. HIV-1 evades innate immune recognition through specific cofactor recruitment. Nature, 2013, 503(7476): 402-405. |
| [49] | Lahaye X, Satoh T, Gentili M, Cerboni S, Conrad C, Hurbain I, El Marjou A, Lacabaratz C, Lelièvre JD, Manel N. The capsids of HIV-1 and HIV-2 determine immune detection of the viral cDNA by the innate sensor cGAS in dendritic cells. Immunity, 2013, 39(6): 1132-1142. |
| [50] | Gao DX, Wu JX, Wu YT, Du FH, Aroh C, Yan N, Sun LJ, Chen ZJ. Cyclic GMP-AMP synthase is an innate immune sensor of HIV and other retroviruses. Science, 2013, 341(6148): 903-906. |
| [51] | Sun CL, Schattgen SA, Pisitkun P, Jorgensen JP, Hilterbrand AT, Wang LJ, West JA, Hansen K, Horan KA, Jakobsen MR, O'Hare P, Adler H, Sun R, Ploegh HL, Damania B, Upton JW, Fitzgerald KA, Paludan SR. Evasion of innate cytosolic DNA sensing by a gammaherpesvirus facilitates establishment of latent infection. The Journal of Immunology, 2015, 194(4): 1819-1831. |
| [52] | Watson RO, Bell SL, MacDuff DA, Kimmey JM, Diner EJ, Olivas J, Vance RE, Stallings CL, Virgin HW, Cox JS. The cytosolic sensor cGAS detects Mycobacterium tuberculosis DNA to induce type I interferons and activate autophagy. Cell Host & Microbe, 2015, 17(6): 811-819. |
| [53] | Wassermann R, Gulen MF, Sala C, Perin SG, Lou Y, Rybniker J, Schmid-Burgk JL, Schmidt T, Hornung V, Cole ST, Ablasser A. Mycobacterium tuberculosis differentially activates cGAS- and inflammasome-dependent intracellular immune responses through ESX-1. Cell Host & Microbe, 2015, 17(6): 799-810. |
| [54] | Collins AC, Cai HC, Li T, Franco LH, Li XD, Nair VR, Scharn CR, Stamm CE, Levine B, Chen ZJ, Shiloh MU. Cyclic GMP-AMP synthase is an innate immune DNA sensor for Mycobacterium tuberculosis. Cell Host & Microbe, 2015, 17(6): 820-828. |
| [55] | Hansen K, Prabakaran T, Laustsen A, Jørgensen SE, Rahbæk SH, Jensen SB, Nielsen R, Leber JH, Decker T, Horan KA, Jakobsen MR, Paludan SR. Listeria monocytogenes induces IFNβ expression through an IFI16-, cGAS- and STING-dependent pathway. The EMBO Journal, 2014, 33(15): 1654-1666. |
| [56] | Storek KM, Gertsvolf NA, Ohlson MB, Monack DM. cGAS and IfI204 cooperate to produce type I IFNs in response to Francisella infection. The Journal of Immunology, 2015, 194(7): 3236-3245. |
| [57] | Zhang YG, Yeruva L, Marinov A, Prantner D, Wyrick PB, Lupashin V, Nagarajan UM. The DNA sensor, cyclic GMP-AMP synthase, is essential for induction of IFN-β during Chlamydia trachomatis infection. The Journal of Immunology, 2014, 193(5): 2394-2404. |
| [58] | Andrade WA, Agarwal S, Mo SY, Shaffer SA, Dillard JP, Schmidt T, Hornung V, Fitzgerald KA, Kurt-Jones EA, Golenbock DT. Type I interferon induction by Neisseria gonorrhoeae: dual requirement of cyclic GMP-AMP synthase and Toll-like receptor 4. Cell Reports, 2016, 15(11): 2438-2448. |
| [59] | Stempel M, Chan BC, Juranić Lisnić V, Krmpotić A, Hartung J, Paludan SR, Füllbrunn N, Lemmermann NA, Brinkmann MM. The herpesviral antagonist m152 reveals differential activation of STING-dependent IRF and NF-κB signaling and STING's dual role during MCMV infection. The EMBO Journal, 2019, 38(5): e100983. |
| [60] | Liu YH, Li JH, Chen JL, Li YM, Wang WX, Du XT, Song WH, Zhang W, Lin L, Yuan ZH. Hepatitis B virus polymerase disrupts K63-linked ubiquitination of STING to block innate cytosolic DNA-sensing pathways. Journal of Virology, 2015, 89(4): 2287-2300. |
| [61] | Ishikawa H, Ma Z, Barber GN. STING regulates intracellular DNA-mediated, type I interferon-dependent innate immunity. Nature, 2009, 461(7265): 788-792. |
| [62] | Nitta S, Sakamoto N, Nakagawa M, Kakinuma S, Mishima K, Kusano-Kitazume A, Kiyohashi K, Murakawa M, Nishimura-Sakurai Y, Azuma S, Tasaka-Fujita M, Asahina Y, Yoneyama M, Fujita T, Watanabe M. Hepatitis C virus NS4B protein targets STING and abrogates RIG-I-mediated type I interferon-dependent innate immunity. Hepatology, 2013, 57(1): 46-58. |
| [63] | Aguirre S, Maestre AM, Pagni S, Patel JR, Savage T, Gutman D, Maringer K, Bernal-Rubio D, Shabman RS, Simon V, Rodriguez-Madoz JR, Mulder LCF, Barber GN, Fernandez-Sesma A. DENV inhibits type I IFN production in infected cells by cleaving human STING. PLoS Pathogens, 2012, 8(10): e1002934. |
| [64] | Sun L, Xing YL, Chen XJ, Zheng Y, Yang YD, Nichols DB, Clementz MA, Banach BS, Li K, Baker SC, Chen ZB. Coronavirus papain-like proteases negatively regulate antiviral innate immune response through disruption of STING-mediated signaling. PLoS ONE, 2012, 7(2): e30802. |
| [65] | Xing YL, Chen JF, Tu J, Zhang BL, Chen XJ, Shi HY, Baker SC, Feng L, Chen ZB. The papain-like protease of porcine epidemic diarrhea virus negatively regulates type I interferon pathway by acting as a viral deubiquitinase. Journal of General Virology, 2013, 94(Pt 7): 1554-1567. |
| [66] | Christensen MH, Jensen SB, Miettinen JJ, Luecke S, Prabakaran T, Reinert LS, Mettenleiter T, Chen ZJ, Knipe DM, Sandri-Goldin RM, Enquist LW, Hartmann R, Mogensen TH, Rice SA, Nyman TA, Matikainen S, Paludan SR. HSV-1 ICP27 targets the TBK1-activated STING signalsome to inhibit virus-induced type I IFN expression. The EMBO Journal, 2016, 35(13): 1385-1399. |
| [67] | Lau L, Gray EE, Brunette RL, Stetson DB. DNA tumor virus oncogenes antagonize the cGAS-STING DNA-sensing pathway. Science, 2015, 350(6260): 568-571. |
| [68] | Clementz MA, Chen ZB, Banach BS, Wang YH, Sun L, Ratia K, Baez-Santos YM, Wang J, Takayama J, Ghosh AK, Li K, Mesecar AD, Baker SC. Deubiquitinating and interferon antagonism activities of coronavirus papain-like proteases. Journal of Virology, 2010, 84(9): 4619-4629. |
 2021, Vol. 61
2021, Vol. 61